





密码过期或已经不安全,请修改密码
修改密码
 添加医院
添加医院


壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





神经调节药物
01
概述
脑肠轴功能紊乱是功能性胃肠病(FGID)重要发病机制之一;
胎儿神经嵴分化为大脑和脊髓,并向下发送神经节填充内胚层,成为肠神经系统。
大脑和肠道共享相同的神经递质和受体,
因此神经调节药物可用于FGID或其他疼痛性躯体症状患者,
无论其是否合并焦虑或情绪障碍。

02
神经调节药物的药理学特性
(1)三环类抗抑郁药(TCA)

点击查看大图
(2)选择性5-HT再摄取抑制剂(SSRI)
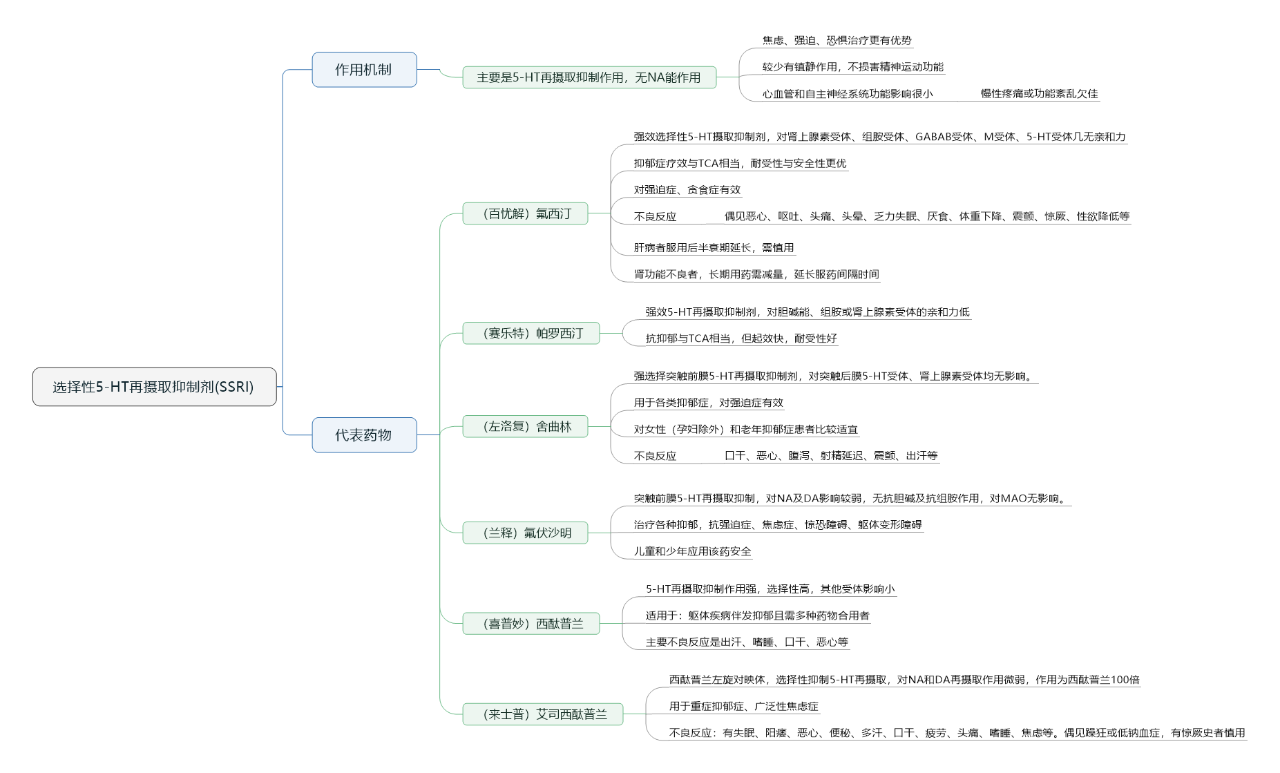
点击查看大图
(3)5-HT及NA再摄取抑制剂(SNRI)
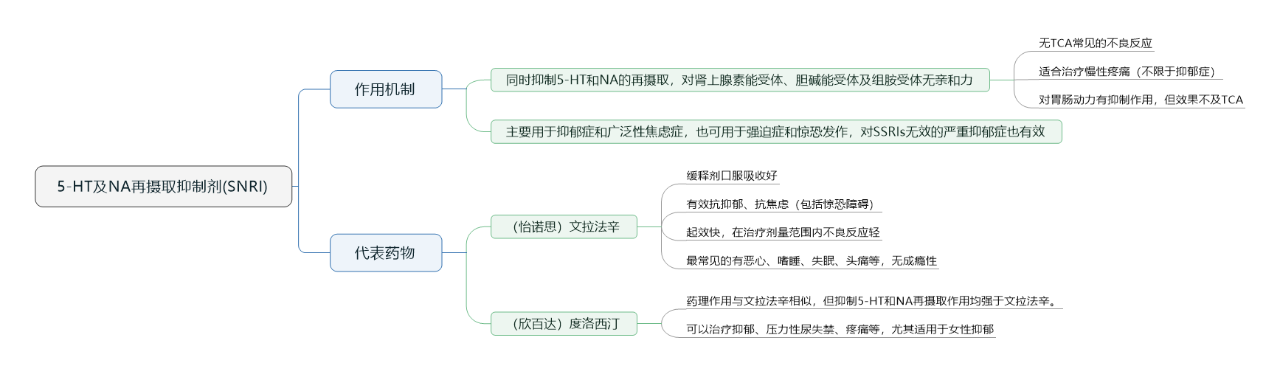
点击查看大图
(4)NA和特异性5-HT能抗抑郁药(NASSA)
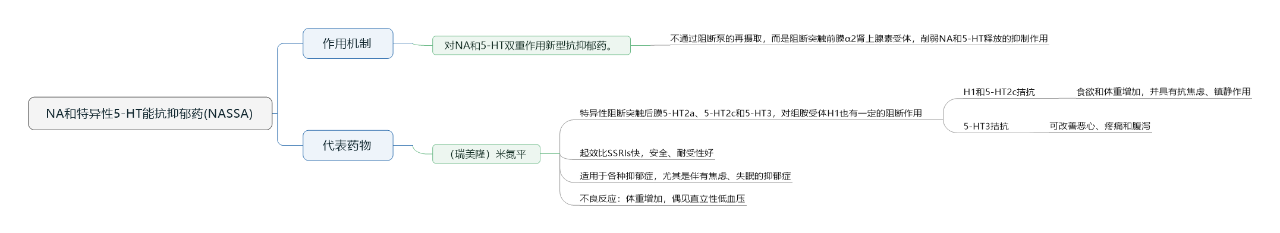
点击查看大图
(5)5-HT1a受体激动剂
作用机制
激动突触前后5-HT1a受体,抑制大脑中的恐惧回路;
也可以通过外周5-HT1a受体直接影响胃肠道生理。
代表药物
丁螺环酮、坦度螺酮,
丁螺环酮增强食管的收缩幅度,并减缓健康对照的胃排空速
率,增强胃容受性,改善症状。
(6)非典型抗精神病药
作用机制
具有多巴胺D2受体拮抗剂(氨磺必利、左舒必利)特性;
具有5-HT2a受体拮抗剂(奥氮平、喹硫平)特性。
长期使用应密切监测不良反应(FGID剂量远低于抗精神病剂量);
左舒必利可降低FD胃扩张的敏感性,偶尔用于治疗FD和胃轻瘫。
(7)α2δ配体
作用机制
外周神经调节剂,用于以疼痛为主的FGID患者;
可能与γ-氨基丁酸(GABA)有关;
也可能与干扰 α2δ亚基钙通道转运,减少脊髓中钙依赖性前痛觉神经递质的释放有关。
代表药物
加巴喷丁、(乐瑞卡)普瑞巴林,
均可增加IBS直肠超敏反应患者的扩张感觉阈值。
03
临床应用
(1)慢性胃肠痛
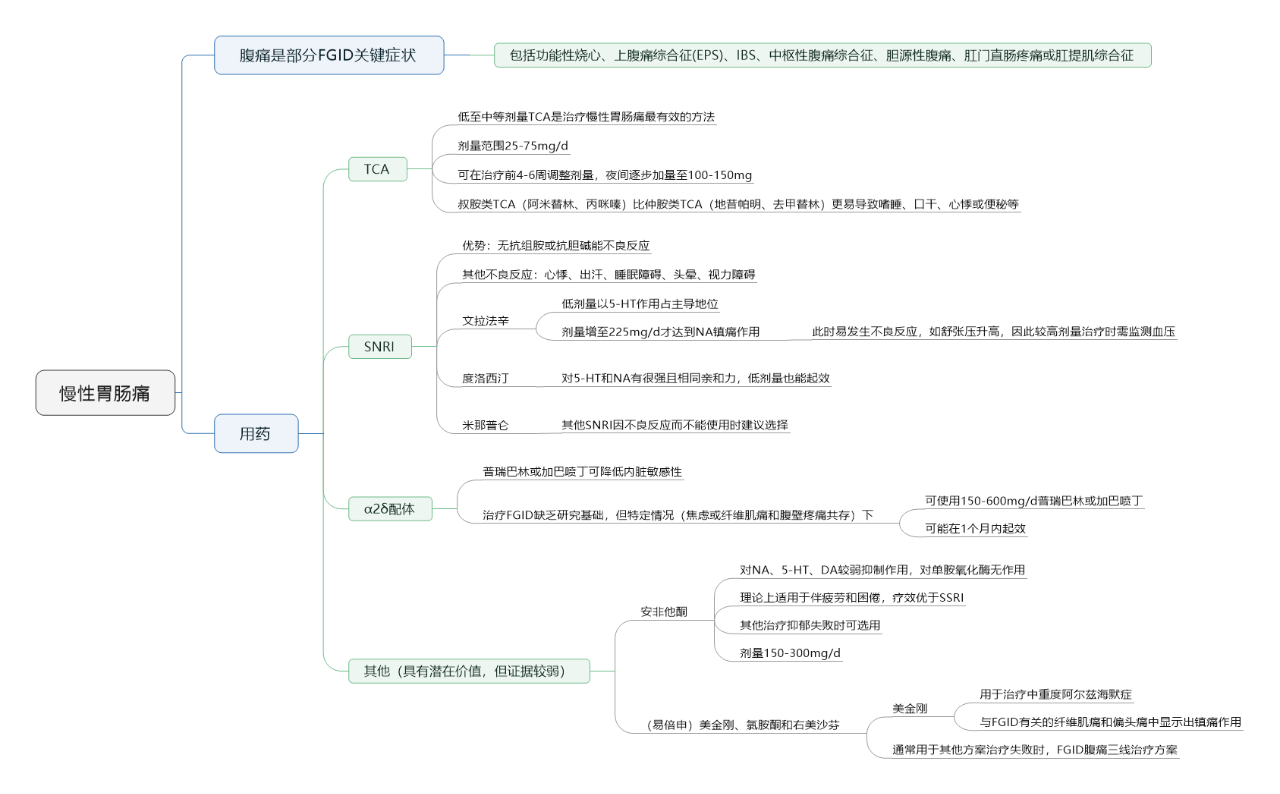
点击查看大图
(2)IBS
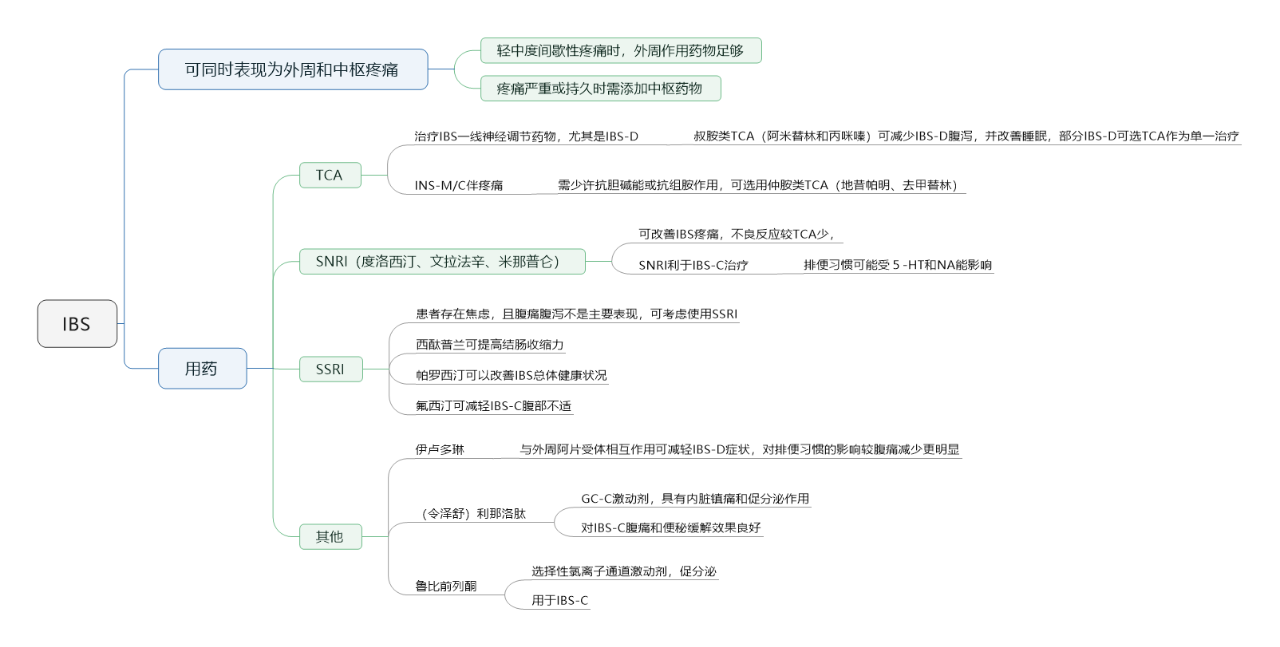
点击查看大图
(3)功能性烧心和功能性胸痛
胃灼热或胸痛在排除GERD时,可考虑使用中枢药物
低剂量TCA(丙咪嗪或阿米替林)
SSRI可用于患有功能性胸痛或食管高敏感的患者,共存的焦虑、抑郁或恐惧
SNRI小剂量(75 mg)文拉法辛仅在一项功能性胸痛研究中优于安慰剂
(4)FD
通过改善生活方式、根除Hp等仍不能控制症状,可使用其他治疗方法
餐后不适综合征(PDS)
丁螺环酮
用于以早饱、腹胀和恶心为主的PDS,不良反较少,无依赖性
剂量:30 mg bid-tid,可增至60mg
米氮平
用于慢性恶心、呕吐或体重减轻PDS,还可改善腹痛症状
剂量:15~45 mg qn,减少对日间影响
奥氮平
米氮平治疗时镇静过度或应答不完全可选择奥氮平
剂量2.5~10 mg/d
上腹痛综合征(EPS)
主要使用TCA(阿米替林),无论发病初期还是PPI治疗失败后
不能耐受TCA治疗也可考虑使用SNRI
(5)周期性呕吐综合征(CVS)
CVS急性发作
昂丹司琼或异丙嗪止吐
可降低症状严重程度并缩短发作持续时间
苯二氮卓类
用于治疗急性焦虑和痛苦,并对减少恶心有独立作用。
预防CVS发作
TCA为预防的一线治疗
联合米氮平,可以缓解恶心和疼痛,减轻焦虑
可使用有止吐作用的奥氮平
TCA治疗失败时,抗惊厥药(唑尼沙胺和左乙拉西坦)治疗有效
04
联合治疗
(1)联合用药
单药治疗失败时推荐联合治疗:
一种外周性药物 + 一种/两种中枢性药物(如非典型抗精神病药加抗抑郁药)联合使用。
特异性药物(TCA、SSRI、SNRI)仅有部分疗效时,可以添加一种药物互补,降低剂量和减少不良反应;
TCA可以缓解部分疼痛,不能控制焦虑,改善睡眠,
可以添加SSRI,
可增加一种非典型抗精神病药物。
联合用药时,注意潜在的不良作用,
5-羟色胺综合征:发热、反射亢进、自发性阵挛、肌肉僵硬。
(2)联合物理或行为治疗
如认知行为疗法(CBT)、肠道定向催眠疗法、正念冥想。
05
补充说明
一般治疗3~4周才起效(部分药物起效很快,如氟哌噻吨美利曲辛片),
治疗4~6周后症状没有改善时需调整药物,
不良反应一般1~2周消失,
药物减量前需要持续治疗6~12月。
作者:陈飞帆
来源:纷飞之翼之住院医师学习笔记






