查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





本文作者:复旦大学附属中山医院肝内科 葛宁灵;复旦大学附属中山医院 海军军医大学东方肝胆外科医院 叶胜龙
在世界范围内,肝细胞癌(HCC)发病率持续增加,针对新疗法的研究也不断面临着挑战。《消化道》(Gut)杂志于2018年2月发表了一份HCC圆桌会议文件[Gut 2018,67:(2):380]。该圆桌会议文件由12位临床和研究背景的国际知名专家,围绕危险因素、肠道微生物群等议题,深入讨论了当前HCC研究的进展、问题和困难。我们特邀复旦大学附属中山医院肝内科葛宁灵主任医师和复旦大学附属中山医院、海军军医大学东方肝胆外科医院叶胜龙教授对这份有关HCC的圆桌会议文件进行解读。敬请关注。
 叶胜龙 教授
叶胜龙 教授
非酒精性脂肪性肝炎、糖尿病和肥胖
要点:
◎ HCC患者中的代谢风险因素特别是糖尿病和肥胖的患病率已经升高。
◎ 对于存在代谢风险因素、但无肝硬化的患者,需要检出HCC的筛查方法。
◎ 对于代谢综合征患者,饮酒对疾病进展和HCC有何重要作用?
解读
近年来,非酒精性脂肪性肝炎(NASH)、糖尿病和肥胖等与HCC相关的代谢性风险因素显著增加,其患病率不断增高,需要引起关注。对存在代谢风险因素而无肝硬化的患者,尚需要能够确定HCC的筛查方法。伴有NASH的HCC患者可能年龄更大、且有更多的并存疾病,预后更差。另一个有待解决的问题是代谢综合征患者饮酒量对HCC病情进展的重要性有多大。
肠道微生物群
要点
◎ 肝硬化与作用广泛的肠道微生态失调有关。
◎ 有关HCC中微生物群的研究尚处于临床前期。
◎ 动物研究已发现益生菌对预防肝癌的发生具有潜在作用。
◎ 人类HCC的发生受肠道菌群影响吗?
解读
肠道微生态稳定对健康机体至关重要,在罹患NASH的人群和肝硬化患者中,均发现存在微生态失调。有关微生物群预测HCC风险、甚或具有治疗的可能作用,目前仍限于临床前研究。
在动物实验中发现肠道微生物群可影响肝癌的发生,抗生素治疗能够抑制肿瘤形成。人类HCC的发生是否受到肠道微生物群的影响,尚有待研究。
分期和预后
要点
◎ 对于患者和研究者,均需要进行疾病分期和预测预后的可靠方法。
◎ 诸如疾病进展时间等生存期的替代指标,并不一定能够转化为总生存期。
◎ 研究应更多地考虑患者在接受治疗的情况下疾病的进展模式。
解读
疾病的分期和预后信息对临床医生确定治疗决策以及研究者设计临床试验方案均具有指导意义。
目前最广泛应用的是巴塞罗那临床肝癌(BCLC))分期和治疗系统,该系统强调总生存期为主要依据。疾病控制或疾病进展时间常用于早期临床试验,但尚无证据显示疾病进展时间在HCC患者中可以替代总生存期。
肝内病灶增大的疾病进展不一定都影响患者预后。索拉非尼的临床试验分析没有发现疾病进展时间和总生存期之间的关系。但是,肿瘤的不同进展模式(如出现肝内病灶的增大或新的肝内病灶,肝外病灶的增大,新的肝外病灶或新的血管侵犯)均可明显影响预后。临床试验设计应更多考虑患者再接受治疗后的疾病进展模式。
生物学标志物以及组织活检
要点
◎ 需要可靠、重复性好的生物学标志物,以提高HCC早期诊断水平和检出亚组患者。
◎ 已经确定分子标签,但尚未完成对其的验证。
◎ 正在研发新的方法,包括基质辅助激光解吸/电离(MALDI)和液体活检技术等。
◎ 除临床试验外,临床医生应常规对肿瘤和周围组织取活检吗?
解读
肿瘤分化和血管侵犯是HCC的组织学预后因素,但肿瘤异质性及术前难以评价血管侵犯等问题影响了肿瘤活检的预测精确性。因此,需要可靠、重复性好的生物标志物来改善对HCC的早期诊断,并检出亚组患者。
根据已确定的分子标签可对HCC进行分组,但尚未完成验证,其原因包括:临床指南并未提倡肿瘤活检;分子标签检测复杂,应用受限;大多数分子标签是在外科切除标本中获得的,是回顾性的,尚不清楚其与原位活检标本的相关性。
除了临床试验之外,临床上是否对肿瘤及周围肝组织进行常规活检仍有争议。
目前HCC的诊断和治疗主要是基于影像学结果,如果影像学检查确定,活检结果将不会改变临床决策。如果影像学检查结果缺乏特异性,则须通过活检来明确诊断。也有人认为活检可获取更多信息,有助于精准治疗。在临床试验中进行活检则有助于识别临床获益的亚组患者。
液体组织活检是检测血浆中的循环肿瘤细胞和核酸的无创新方法。循环肿瘤细胞的存在与总生存期短、疾病复发和死亡风险升高相关。但对此尚需要进一步验证,对假阳性结果也需要解释。
综合应用影像学、病理学结果及临床标记可能是对HCC患者更好的分层途径。目前尚无确认的有用生物学标志物,前瞻性活检样本研究是今后的方向。
局部区域治疗
要点
◎ 消融用于治疗小肿瘤(<3 cm)最为成功,射频消融是最常用的消融技术。
◎ 对于不能切除的肝细胞癌(HCC),采用经肝动脉化疗栓塞术进行栓塞治疗,显示有生存优势。
◎ 放疗栓塞是替代选择,但是尚未表明其带来的生存获益优于经肝动脉化疗栓塞术。
◎ 对于中期HCC,如何开展有关总生存期的研究?
解读
消融和栓塞是常用的HCC局部区域治疗。
对于小肿瘤(直径<3 ~ 4 cm),消融治疗可以替代手术切除作为一线治疗。射频消融最为常用。其他还有微波、冷冻和不可逆电穿孔消融,微波或可改善较大肿瘤的消融效果,冷冻和不可逆电穿孔没有热损伤,但尚需要更多临床数据来确立它们的治疗价值。
栓塞治疗包括多种技术,广为应用的常规化疗栓塞是经动脉化疗栓塞术,经研究证实,对于不能切除的肝癌患者,经动脉化疗栓塞可带来生存获益。药物洗脱微球经动脉化疗栓塞术和钇90放射性栓塞术是近年应用的栓塞新技术,目前尚未证实比常规经动脉化疗栓塞术有更好的生存获益。较晚期的患者对药物洗脱微球经动脉化疗栓塞术的耐受性较好。放射性栓塞术可用于将伴有肝硬化的、不能接受手术切除的患者过渡至可接受手术切除。
如何有效提高局部区域治疗总体生存疗效,目前尚有待进行深入研究。
联合治疗
要点
◎ 应用联合治疗方法的成败参半,但是,尚未表明射频消融/切除+索拉非尼以及经动脉化疗栓塞术+索拉非尼可以延长生存期。
◎ 这些失败的结果提示需要重新考虑联合治疗的概念。
◎ 序贯应用各种疗法是否优于同时联合应用各种疗法吗?
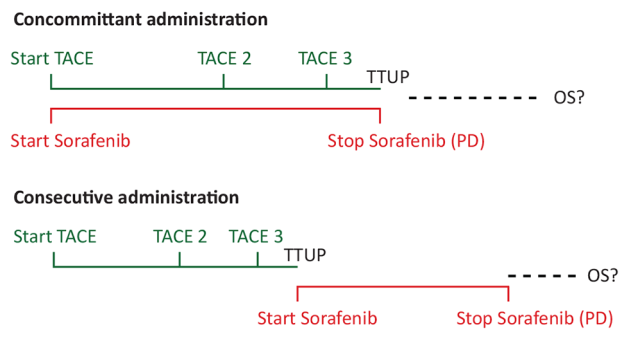
“TACE and sorafenib: combine, but how? OS, overall survival;PD, progressive disease; TTUP, time to untreatable progression.”
解读
HCC联合治疗方法成败参半。
手术切除、射频消融或经动脉化疗栓塞术联合索拉非尼治疗的临床试验均未能证实可延长患者的总生存期或疾病进展时间,这提示需要重新思考联合治疗的概念。
没有证据表明同时应用的联合药物治疗比序贯治疗有更好的总生存期获益。也没有证据表明两种药物比单一药物的疗效更好。目前,只有索拉非尼与瑞戈非尼的序贯治疗确实改善了患者的生存。
有关射频消融联合经动脉化疗栓塞术临床试验的荟萃分析表明,总生存期和无复发生存期仅在肿瘤>3 cm的患者中有显著改善,对于小肿瘤进行射频消融,不需要联合经动脉化疗栓塞术。肝移植前经动脉化疗栓塞术是成功的辅助治疗方法。
如何有效进行HCC的联合治疗以及同时应用或序贯治疗两者孰优孰劣,仍有待更多临床实践的验证。
为什么有前景的化合物治疗失败?
要点
◎ 患者的选择是研究的关键,这有助于将抗肿瘤效果转化为患者生存期的延长,患者需要良好的肝功能和体能状态。
◎ 药物的毒性至关重要,关于这一限制性因素,Ⅱ期试验尚未给出足够有力的充分信息。
◎ Ⅱ期试验中的疾病进展时间和治疗应答并不是足够有用的治疗成功标志物,应该考虑应用症状进展、进展模式和总生存期作为治疗成功的标志物。
◎ 应该考虑进行Ⅱ期随机对照试验,这些试验应该利用分层方法,以确保治疗分组的适当均衡。
◎ 对“所有参与者”进行的试验可能将不再合适,未来可能在于治疗由肿瘤和周围组织的分子生物学和遗传学特征所定义的亚组患者。
解读
目前虽已研发许多新药,但多数药物Ⅲ期临床试验结果均告失败,其原因在于:疗效未达预期;患者不可耐受的毒性;试验设计不合适,尤其是不同试验组的预后相关因素不均衡。
索拉非尼临床试验的经验表明,患者选择是成功的关键。肝功能、体能状况与肿瘤负荷都可能影响预后,随机对照临床试验需要仔细选择病例,确保治疗分组的均衡。
药物的毒性是限制性因素,而Ⅱ期临床试验未能提供充分有力的信息。Ⅱ期临床试验应考虑采用至症状进展、进展模式和总生存期作为治疗成功的标志。
对“所有参与者”进行的临床试验变得不再合适,将来的临床试验可能需要针对亚组患者进行治疗,而这些亚组患者是由肿瘤本身和周围组织的分子生物学和遗传学特征所定义的。
免疫肿瘤学
要点
◎ 免疫疗法不受患者肝功能影响。
◎ 早期研究显示一些免疫疗法取得某些成功。
◎ 免疫疗法应与局部治疗和(或)索拉非尼联合应用吗?
解读
免疫治疗在癌症治疗中最受关注。免疫治疗不涉及代谢,其应用不受肝功能影响,已与消融治疗联合应用于早期HCC。其概念为应用包括阻断免疫检查点和免疫抑制细胞因子等多种机制来激活T细胞,增强抗肿瘤作用。
免疫检查点抑制剂治疗在多种癌症中试验成功,现正在引入到HCC治疗中。已有报告应用免疫检查点抑制剂[抗细胞毒性T淋巴细胞相关抗原4(CTLA-4)单抗和抗程序性死亡受体1(PD-1)单抗]的早期HCC免疫治疗试验。细胞因子激活的杀伤细胞初步观察也有成效。嵌合抗原受体T细胞(CAR-T)、溶瘤病毒和肿瘤疫苗的试验研究更为引人关注。此外,肝脏还可提供多种靶点,包括T细胞、免疫细胞死亡、增强抗原提呈细胞功能、巨噬细胞、细胞因子和趋化因子等。
分子标签检测可能有助于识别对免疫治疗有反应的患者;目前免疫治疗在HCC中的初步应用为不能耐受索拉非尼的患者的替代治疗;免疫治疗与射频消融、切除、经动脉化疗栓塞术或索拉非尼联合应用是否有生存获益的研究正在进行或将开展。
个性化治疗的新靶点和策略
要点
◎ 基因测序已确定靶向HCC的6个相关区域。
◎ 需要对肿瘤进行测序,提高对疾病的认识。
◎不应将tivantinib的阴性结果外推至其他MET抑制剂治疗。
◎ 如何更好地描述突变结果的特征,以确定治疗靶点?
◎ 肿瘤异质性有何影响?如何处理该影响?
◎如何研发针对HCC主要遗传学改变的新的靶向治疗?
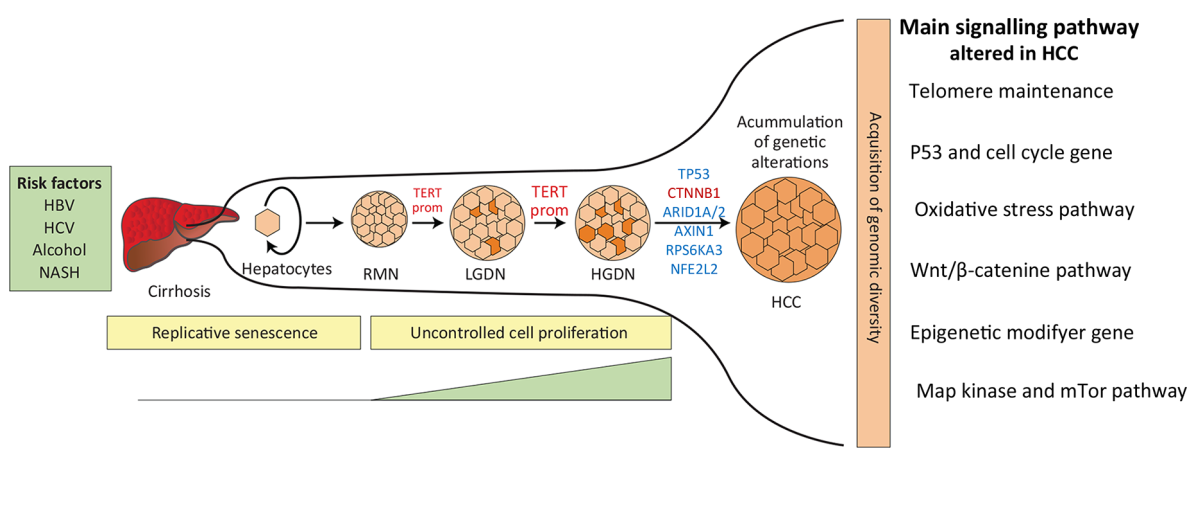
解读
基因测序提示每个肿瘤有4 ~ 6个靶向关键信号通路的驱动功能突变参与肝脏癌变。6个相关区域的基因突变与靶向HCC有关:端粒维持、细胞周期基因和P53通路、氧化应激通路、Wnt/β-联蛋白通路、表观遗传学修饰以及丝裂原激活蛋白激酶与哺乳动物雷帕霉素靶蛋白(mTOR) 通路。但这些确定的基因突变却与目前HCC的治疗靶点无关。
基因测序有利于更好地理解肿瘤、开发新疗法和预测对系统治疗应答或抵抗的生物学标志物。为此,在临床试验中必须进行肿瘤活检和建立生物库,理想的是在临床试验前获取组织样本。
深入理解基因突变结果的特征,以确定治疗靶点、处理肿瘤异质性的影响及研发针对HCC主要基因改变的新的靶向治疗,是当前HCC研究必须应对的挑战。
(要点翻译:张福奎)
《中国医学论坛报》2018年4月5日 D1、D4版
查看更多