查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





作者:北京大学人民医院、北京大学肝病研究所魏来教授

魏来教授
2017年慢性丙型肝炎抗病毒治疗的进展主要集中于“消除丙型肝炎公共卫生威胁”的目标,在多个层面和多个方向的进展都使我们更接近这个目标。
WHO发布《全球肝炎报告》:形势严峻,目标明确,分享经验
世界卫生组织(WHO)在2017年发布了《全球病毒性肝炎报告》,主要包括以下6个方面。
1. 病毒性肝炎是一个需要紧急应对的主要公共卫生问题。
2. 接种疫苗可以大大减少儿童新发乙肝病毒(HBV)感染, 不过,预防HBV和丙肝病毒(HCV)的其他措施尚没有得到充 分实施。
3. 由于成人慢性感染负担重,需要使检测和治疗的获得更为便利。
4. 较早采纳相关措施的国家正在迈向消除病毒性肝炎。
5. 目前存在采取立即行动的机会,例如,通过扩大对合并感染HBV或HCV的艾滋病毒感染者的治疗。
6. 要达到2030年消除病毒性肝炎的目标,就要大规模地采用全面的公共卫生方法。
WHO这份报告的第1条就指出,病毒性肝炎是一个需要紧急应对的主要公共卫生问题。在2015年,病毒性肝炎导致了134万人的死亡,该数据大于艾滋病导致的死亡人数。随着时间的推移,病毒性肝炎导致的死亡数量正在增加。
据估计,2015年全世界有7100万人存在慢性HCV感染。HCV感染导致的丙肝流行影响所有WHO的区域,其中在国家之间和各国内部差异巨大。
关于病毒性肝炎的预防,该报告指出,虽然注射和吸毒是一些地区HCV传播的主要路径,但是,这些地区尚未充分提供有效减少这些危害的服务。全球仍有5%的卫生保健相关注射不安全。据估计,以上原因造成2015年全球发生175万例新发HCV感染。这两个感染途径也是我国预防HCV新发感染的重要问题。
在检测和治疗方面,WHO的报告提出,若干较早采纳相关措施的国家的实践表明,通过政治领导人做出承诺以及降低基本药物和诊断制剂的价格,可以快速扩大检测和治疗服务。
使用高度有效的直接抗病毒药物(DAA)可以在2~3个月内治愈丙型肝炎,而且,在一些国家,只需要花费200美元,就可获得全疗程所需要的仿制直接抗病毒药物。
世界肝炎峰会:呼吁加速行动,弥合缺口,创新方法与措施,消灭病毒性肝炎
2017年10月31日,在巴西圣保罗市召开的世界肝炎峰会的前夕,WHO所收到的各方报告显示,过去5年内,制定本国消除危及生命的病毒性肝炎计划的国家数增加近5倍。过去2年内,共有300万人获得了丙肝治疗。2016年全球共有194国政府决定到2030年消除病毒性肝炎。2016年接受丙型肝炎抗病毒治疗人数新增176万人,显著高于2015年的110万人。
但是,仍然存在一些挑战。大多数国家缺乏足够的资金来提供重要的肝炎防治服务;关于诊断方面,2015年,只有1/5的HCV感染者知道自己已经受到感染。各国需要改进其相关政策和规划,以提高对HCV感染的认识,并作出诊断。
在预防领域,各国需要向各类人群、特别是感染风险较高人群提供全方位的肝炎预防服务。
在世界肝炎峰会上,各全球伙伴重申承诺,争取到2030年实现消除病毒性肝炎的目标。
中国加快消除丙肝步伐:提出2030年消除丙肝危害的目标
2017年11月14日,国家卫生计生委、国家发展改革委、教育部、科技部、工业和信息化部、公安部、财政部、人力资源社会保障部、住房城乡建设部、国家食品药品监管总局和国家中医药管理局等11个部门联合发布了《中国病毒性肝炎防治规划(2017-2020年)》。
在该规划中,关于丙肝防控的具体目标是,到2020年,血站的血液HCV检测率达到100%。
《中国病毒性肝炎防治规划(2017-2020年)》同时还提出,医疗机构要落实手术、住院、血液透析、接受有创诊疗患者的丙型肝炎检查。并提出医疗卫生机构和体检机构在知情同意的前提下,开展丙型肝炎的筛查。还提出对病毒性肝炎药品进行集中采购,以保证药物治疗的可及性。
虽然该规划的篇幅乃至具体目标更多的是覆盖了乙型肝炎,但是,这是我国政府第一次对于丙型肝炎的防控提出了具体目标。其他一些具体要求将有利于丙型肝炎防控工作的开展和落实。
该规划的更进一步的进展是,在2018年国家卫生计生工作重点任务第2条关于预防控制重大疾病中强调,启动实施中国2035年终结结核病和2030年消除丙型肝炎危害两大行动。
HCV感染诊断:更加规范,更加便捷及快速
2017年2月,亚太肝脏研究学会(APASL)第26届年会在我国上海举行,会议期间,WHO正式发布了第一部《病毒性肝炎检测指南》。该指南对于丙肝病毒(HCV)感染的检测包括了以下2点: ① 各个国家建立自己的国家病毒性肝炎检测政策、管理机制和参考实验室;② 给予财政预算,人力资源配备,监测检测质量,实施质量控制。
该指南强烈推荐对于感染人群进行检测,包括来自高流行区,或有高危行为或有暴露史的成人和青少年人群;以及临床怀疑HCV感染的成人和儿童。
关于有条件推荐,该指南指出,在一般人群,可利用现有条件或人类免疫缺陷病毒(HIV)/结核防控体系进行丙型肝炎检测。
对于接受抗病毒治疗的人群,指南强烈推荐在资源有限的地区进行快速检测,有条件推荐在抗-HCV阳性情况下检测HCV核酸或者HCV核心抗原,在抗病毒治疗结束12周或24周进行检测,以确定是否获得治愈。
2017年,澳大利亚的一个多中心研究报告了一个床旁快递检测HCV RNA的Xpert检测方法。该研究纳入5个中心的感染者队列:3个静脉用药成瘾和酒精依赖中心、1个流浪者服务中心和1个注射针头交换项目。
研究者以雅培实时(RealTime)HCV检测为金标准,评价Xpert检测指血和真空采血管采血HCV RNA的敏感性和特异性,150例感染者中RealTime 检测HCV RNA阳性5例,Xpert检测真空管采血HCV RNA的敏感性为100.0%,特异性为99.1%;检测指血的敏感性为95.5%,特异性为98.1%。如能经过更多基因型、更广泛区域的验证,将有助于提高抗病毒治疗监测的可及性,继而提高抗病毒治疗可及性。
抗HCV治疗:DAAs治疗覆盖人群更广,难治人群进一步减少
2017年,美国食品药物管理局(FDA)批准了索磷布韦(sofosbuvir)联合velpatasvir/voxilaprevir用于慢性丙型肝炎直接抗病毒药物(DAAs)经治失败的人群,包括基因1型至基因6型HCV感染;批准了glecaprevir联合pibrentasvir治疗基因1~6型伴有或者不伴有肝硬化的慢性丙型肝炎。
2017年DAAs治疗的人群的研究主要新增了以下几种。
1. 索磷布韦联合velpatasvir/voxilaprevir用于慢性丙型肝炎NS5A抑制剂经治失败的人群。
2. Glecaprevir联合pibrentasvir治疗基因1~6型伴有或者不伴有肝硬化的慢性丙型肝炎。
3. Glecaprevir联合pibrentasvir用于慢性丙型肝炎NS5B抑制剂经治失败的人群。
4. 索磷布韦联合ledipasvir用于基因1型伴严重肾功能损伤的患者。
5. Elbasvir联合grazoprevir用于慢性丙型肝炎伴有肾脏损伤者。
6. Elbasvir联合grazoprevir 8周疗程用于初治基因1型,不伴严重肝纤维化的慢性丙型肝炎。
7. 索磷布韦联合ledipasvir用于12岁以上青年,以及6岁以上儿童。
8. 索磷布韦联合ledipasvir用于HIV感染发生急性HCV感染。
9. 索磷布韦联合ledipasvir用于基因1型HCV以及HBV合并感染的人群。
其中最为重要的突破是针对DAAs耐药患者的新DAAs方案,新方案的诞生为DAAs治疗失败提供了解决方法。
另一个重要的突破就是,索磷布韦联合ledipasvir用于基因1型伴有严重肾功能损伤的患者,这一突破使得最后一个没有被DAAs覆盖的人群获得了治疗的DAAs治疗的安全性和有效性数据,那就是肝硬化失代偿合并严重肾功能损伤的慢性丙型肝炎患者。
以往含有蛋白酶抑制的几个方案可以用于慢性肾脏疾病以及严重肾功能损伤的患者,但不能用于肝硬化失代偿的患者。而索磷布韦以往可以用于肝硬化失代偿的患者,但缺少用于严重肾功能损伤的患者的研究数据。
中国抗HCV治疗:多个DAAs获批,可覆盖广泛的感染人群,部分省份快速纳入医保
2017年4月,我国批准了第一个直接抗丙型肝炎药物,阿舒瑞韦联合达拉他韦治疗基因1b型慢性丙型肝炎的方案。
随后于2017年9月我国批准了索磷布韦联合利巴韦林联合或不联合聚乙二醇干扰素α治疗基因1~6型的慢性丙型肝炎患者,以及奥比帕利联合达塞布韦治疗基因1型慢性丙型肝炎患者。
这些药物在我国的获批,标志着我国丙型肝炎治疗真正进入了DAAs时代。
其中,阿舒瑞韦联合达拉他韦适用于基因1b型慢性丙型肝炎患者,奥比帕利联合达塞布韦治疗基因1型慢性丙型肝炎患者,这两个方案均可应用于合并慢性肾脏疾病(CKD)的慢性丙型肝炎患者,乃至CKD 5期[估计的肾小球滤过率(eGFR)低于30 ml/(min·1.73 m2]的慢性丙型肝炎患者。
索磷布韦联合利巴韦林联合或不联合聚乙二醇干扰素α适用于多个基因型的患者,可应用于肝功能失代偿患者。
而且,这些DAAs的批准,还带来了两个潜在的意义,一个是达拉他韦联合索磷布韦组合对多个基因型有效,为利巴韦林不耐受或者基因3型等难治患者提供了可选方案;另一个就是具备了蛋白酶抑制剂、NS5A磷酸化抑制剂以及NS5B RNA依赖的RNA聚合酶抑制剂三个靶点。因此,对于既往经其他途径治疗失败的患者,可以通过三个靶点药物的组合来进行治疗。
表 国产DAAs方案的靶点和目前进展情况
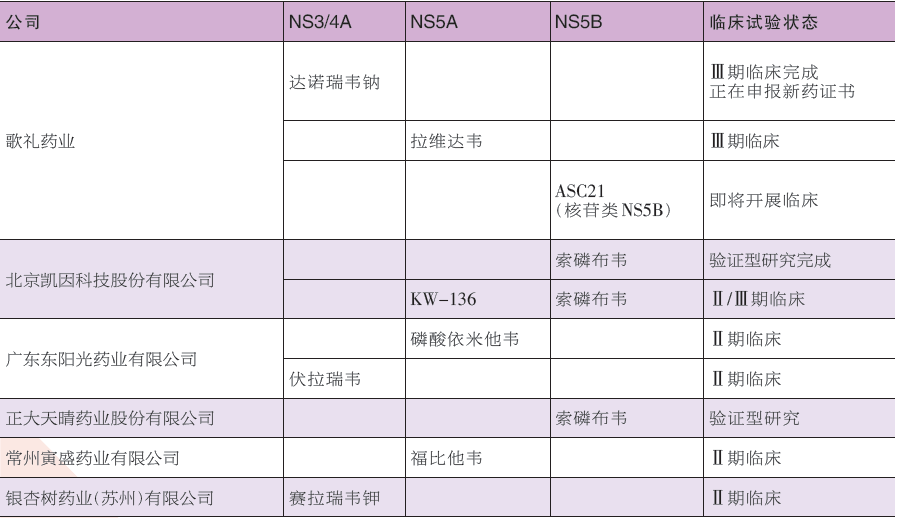
2017年2月,在DAAs获批不到1年的时间内,浙江省在全国率先将抗丙型肝炎DAAs纳入纳入大病保险特殊药品政府谈判。并在谈判后将阿舒瑞韦、达拉他韦和索磷布韦3个药物纳入最终名单。随后,吉林省也将DAAs纳入医保。
相信今后其他省市可参照浙江的方式进行,从而提高抗丙型肝炎治疗的药物可及性。
国产原研的DAAs在2017年有多个方案顺利进行或启动临床药物试验。杭州歌礼的丹诺瑞韦等待批准上市。
展望2018年
2018年的主要发展将会表现在以下几方面:
·在抗病毒治疗方案方面主要是部分DAAs方案的8周疗程、无干扰素无利巴韦林的全基因型。
·获得更多的真实世界的数据。
·在药物可及性方案,有可能实现国家谈判和集中采购,并可能纳入更多地区的医保体系。
《中国医学论坛报》 2018年3月22日 D1~D2版
查看更多