查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





终末期肝病(end-stage of liver disease,ESLD)指各种慢性肝脏损伤所致的肝病晚期阶段,包括慢加急性肝衰竭(acute-on-chronic liver failure,ACLF)、肝硬化急性失代偿(acute decompensation of liver cirrhosis,ADC)、慢性肝功能衰竭(chronic liver failure,CLF)和肝细胞癌(hepatocellular carcinoma,HCC)。
ESLD患者合并感染是其最常见的并发症,ESLD患者常因此病情加重甚至死亡。ESLD合并感染的早期诊断和正确及时的治疗是肝病感染专业极为重要的临床问题。2018年,宁琴教授、王贵强教授牵头国内40余位专家,出台了国内首个针对“终末期肝病合并感染”诊断和治疗的专家共识,该共识在临床的推广应用极大提高了我国广大临床一线医师对于该疾病的规范化诊疗能力。
随着临床研究的深入,更多更新的循证医学证据发表,为更好地指导临床医师诊疗,宁琴教授再次组织相关专家对共识进行了修订(2021版)。在2022年中华医学会第十七次全国感染病学术会议上,赵彩彦教授对其中重要内容进行了解读,概要总结如下。
作者:河北医科大学第三医院 赵彩彦 魏梦平

赵彩彦教授
目前,ESLD合并感染以自发性细菌性腹膜炎(spontaneous bacteria peritonitis,SBP)最多见,其次是肺部感染、尿路感染、皮肤软组织感染等。以大肠埃希菌、肺炎克雷伯菌等革兰阴性菌为主要病原体,但革兰阳性菌和多重耐药菌占比不断增加,尤其在与医疗保健相关的环境中。因此开展经验性抗感染治疗前需明确当地优势菌群和耐药情况。
免疫系统在ESLD合并感染的发生发展过程中至关重要。肝硬化相关免疫功能障碍((cirrhosis-associated immune dysfunction,CAID)是ESLD的病理生理基础,其一是获得性免疫缺陷,即肝脏局部免疫监视功能受损(肝窦纤维化及毛细血管化、纤维间隔伴门体分流形成、Kupffer细胞减少)、表达于固有免疫细胞上的模式识别受体合成减少、循环免疫细胞功能受损(中性粒细胞吞噬、黏附功能下降、单核细胞Fc-γ受体功能障碍、记忆B细胞功能异常、NK细胞对细胞因子刺激应答减弱等);其二是系统性炎症,即坏死肝细胞释放损伤相关分子模式(damage-associated molecular patterns,DAMP)持续间歇性活化循环免疫细胞,使中性粒细胞CD11b、单核细胞表面HLA-DR、T淋巴细胞表面活化抗原等表达上调,进而升高血清促炎细胞因子水平;随疾病进展,肠道菌群失调,肠上皮完整性和全身免疫防御功能受损,并且CAID导致的高促炎细胞因子水平通过影响血流动力学及血管张力增加肠道通透性,使来自肠道细菌的病原相关分子模式(pathogen-associated molecular patterns,PAMP)进一步激活免疫系统,加重全身炎症。
CAID随ESLD疾病阶段不同而动态演变:在肝硬化进展的早期阶段,免疫系统因PAMP的频繁刺激而呈现“促炎”状态;刺激持续使得免疫应答发生再编程,随疾病进展至严重肝硬化失代偿阶段而转至“免疫缺陷”状态;继续进展至ACLF阶段则呈现出类似于脓毒症的“免疫麻痹”状态,表现为单核细胞上抗原递呈HLA-DR分子表达减少,单核细胞产生肿瘤坏死因子-α功能障碍、T淋巴细胞γ干扰素产生减少,促炎及抗炎细胞因子大量释放,导致ESLD患者易发生感染、对病原菌刺激低应答以及多器官功能障碍,死亡率高。
ESLD合并感染时因原发病的影响和患者免疫功能低下临床表现常不典型,需仔细甄别,早期发现,及时治疗。当出现以下表现时,需要高度关注是否合并感染:
1. 原有肝病症状加重,常出现乏力,腹胀、精神萎靡或较前加重;
2. 低热,或不发热;
3. 白细胞较患者基础值升高,中性粒细胞升高;
4. C反应蛋白(C-reactive protein,CRP)/降钙素原(procalcitonin,PCT)或其他炎症因子升高;
5. 肾功能恶化;
6. 其他局部表现如呼吸道症状、腹部症状或泌尿道症状。
所有ESLD患者入院时均应除外感染。ESLD合并感染多起病隐匿且症状不典型,伴CRP、PCT合成功能下降,临床表现及实验室检查诊断价值有限。病原体诊断是ESLD合并感染的“金标准”,传统微生物培养方法操作复杂、耗时长,并且病毒、非典型病原体等无法用常规方法培养,而宏基因组新一代测序技术(metagenomics next-generation sequencing,mNGS)可以直接对临床样本中的核酸进行快速高通量测序,并与已知微生物序列数据库比对,从而明确样本包含的病原微生物种类及占比。mNGS准确性高、能检测到传统手段无法检测到的病原体,同时获取其血清型、毒力特征和耐药情况。因此,本共识纳入mNGS以提高ESLD合并感染的病原体检出率。但mNGS不能区分定植和感染,因此解读mNGS结果应结合患者临床表现及相关化验检查。若mNGS阴性,不能完全排除感染,需结合临床表现,综合分析,做出正确的诊断和治疗。
ESLD合并感染患者的营养状态与其预后密切相关,因此ESLD合并感染患者应进行营养筛查及营养风险评定,明确有无营养不良及其程度,必要时给予营养干预以改善临床结局。
常用的营养筛查方法包括体质指数(body mass index,BMI)、Child-Pugh分级、营养风险筛查(nutrition risk screening,NRS)2002和英国皇家自由医院营养优先排序工具(royal free hospital-nutritional prioritizing tool,RFH-NPT)等。NRS 2002筛查ESLD患者的准确性欠佳,可能与ESLD常合并各种并发症有关。相比之下,RFH-NPT更适用于ESLD患者,准确度更高。筛查结果为BMI<18.5 kg/m2、Child Pugh C级、NRS 2002总分>3分、RFH-NPT>2分提示高营养不良风险。
对存在营养风险患者的评定内容包括肌肉质量和功能评估、主观全面评定、肝病营养评定和饮食摄入量评估。基于计算机断层扫描技术获取第三腰椎水平横断面肌肉面积,从而计算第三腰椎水平骨骼肌指数(L3-skeletal muscle index,L3-SMI)以评估骨骼肌肌量,男性<50 cm2/m2,女性<39 cm2/m2考虑为肌少症。握力测定可评价肌肉功能,静息状态下,男性>25 kg,女性>18 kg则可排除肌少症。在主观全面评定法基础上增加BMI、上臂肌围、进食情况这些客观指标,以此形成的英国皇家自由医院整体评价量表(royal free hospital-global assessment,RFH-GA)判断ESLD患者营养状态更准确。
对营养状态欠佳的患者给予相应营养干预,旨在保证适度能量和充足蛋白质的摄入。ESLD营养不良、肌少症患者大多能量摄入不足,考虑静息能量消耗、食物产热与身体活动相关能量消耗,需25~35 kcal/(kg·d),其中蛋白质或氨基酸需1.2~1.5 g/(kg·d)以保证足够的氮摄入量并防止加剧肌少症,可口服营养补充剂和支链氨基酸补充剂,仍不足时予短期肠内营养或补充性肠外营养。肥胖患者(干体质量BMI>30 kg/m2)可适度低能量摄入25 kcal/(kg·d),但需保证足够的蛋白质摄入>1.5 g/(kg·d),在不影响蛋白质储存的情况下控制体重。此外,ESLD患者肝脏合成、储存糖原减少,糖异生增加,易出现空腹低血糖,应少食多餐(4~6餐/d)、睡前加餐以避免长时间空腹分解体内脂肪及蛋白质。ESLD患者肠内营养及睡前加餐,有助于提高血浆白蛋白水平,改善患者的营养状态。
白蛋白可以改善有效血容量,预防腹水、细菌感染等多种肝硬化并发症,但预防性使用仅能提高肝硬化合并SBP患者的生存率。因此,ESLD合并感染患者应积极纠正低蛋白血症,同时考虑到丙种球蛋白可迅速提高血清免疫球蛋白G水平,胸腺肽α1可促进T淋巴细胞成熟及分泌,必要时可用于增强机体抗感染和免疫调节功能。
ESLD患者常合并脾功能亢进与骨髓造血功能低下,加之肝功能严重受损时肝脏产生血小板生成素(Thrombopoietin,TPO)显著减少,导致血小板生成减少,所以ESLD合并感染患者易出现血小板减少症,即血小板< 100×109/L。临床上维持血小板计数> 50×109/L可降低出血风险。除输注血小板,还可应用升血小板药物作为血小板输注的替代治疗。TPO受体激动剂阿伐曲泊帕,已获FDA批准用于慢性肝病患者相关血小板减少症,疗效显著,耐受性及安全性良好。此外,治疗血小板减少症可能有助于改善肝功能,可能的机制为血小板可释放肝细胞生长因子和胰岛素样生长因子1、刺激肝窦内皮细胞从而诱导肝细胞再生。
ESLD合并感染因病情复杂预后差,要结合患者可能的病原体、感染的部位、感染来源、肝肾功能情况、既往抗菌药物应用史、结合本医疗机构耐药菌情况,选择尽可能覆盖可能病原体的杀菌剂,必要时要联合用药。
病原体多来源于肠道,以大肠埃希菌、肺炎克雷伯菌等革兰阴性菌为主,其次是革兰阳性球菌,以屎肠球菌、粪肠球菌为主。经验性抗感染治疗应以革兰阴性菌为主,若为社区获得性,细菌耐药率较低的地区首选第三代头孢菌素,细菌耐药率较高的地区则可选用哌拉西林/他唑巴坦;若为医院获得性,超广谱β-内酰胺酶(extended-spectrum β-lactamase,ESBL)阳性率高,应选用碳青霉烯类抗感染治疗,在革兰阳性菌多重耐药高发区或合并脓毒症时,需考虑合并耐药革兰阳性球菌感染,联用万古霉素或利奈唑胺,应用万古霉素前需检测肾功能,利奈唑胺有骨髓抑制的副作用,需谨慎选用。
若为社区获得性,以革兰阳性菌为主,选用青霉素/β内酰胺酶抑制剂、一二代头孢菌素,考虑老年人、有基础疾病时,还可选用呼吸喹诺酮类、第三代头孢菌素或厄他培南;若为医院获得性,轻中症感染仍可用青霉素/β内酰胺酶抑制剂,青霉素过敏者调整为碳青霉烯类,重症感染时需考虑铜绿假单胞菌等革兰阴性杆菌可能,选用碳青霉烯类,存在混合感染时联用糖肽类或利奈唑胺。
单纯性下尿路感染病原体以革兰阴性杆菌为主,大肠埃希菌占80%以上,经验性抗感染治疗时,若为社区获得性,则ESBL阴性大肠埃希菌可能性大,轻症首选呋喃妥因、氟喹诺酮类亦有效(莫西沙星因尿液中浓度低须除外);若为医院获得性,则ESBL阳性肠杆菌属可能性大,阿莫西林/克拉维酸、哌拉西林/他唑巴坦均有良好抗菌效果。复杂性尿路感染病原体耐药率高,仍以革兰阴性菌为主,肠球菌较单纯性尿路感染占比增加,经验性抗感染治疗时,若为社区获得性,第三代头孢菌素可用于ESBL阴性肠杆菌,哌拉西林/他唑巴坦、厄他培南可用于ESBL阳性肠杆菌;若为医院获得性,混合感染可能性大,在碳青霉烯类基础上联合对耐药革兰阳性菌有效的糖肽类。此外,对于上尿路感染或合并脓毒症,考虑多为ESBL阳性肠杆菌,首选碳青霉烯类。
ESLD合并继发性血流感染,约60%归因于革兰阴性菌,与肠道细菌移位有关,随细菌耐药率升高,β-内酰胺/β-内酰胺酶抑制剂组合和碳青霉烯类被广泛用于治疗肝硬化合并革兰阴性菌血流感染。此外,β-内酰胺与碳青霉烯类均为时间依赖性抗菌药,与间歇(推注)输注相比,哌拉西林-他唑巴坦或碳青霉烯类药物的持续或延长输注显著提高了PK/PD达标率和患者生存率,因此建议感染早期用于经验性治疗。对于ESLD合并感染性心内膜炎的经验性抗感染治疗,应覆盖敏感及耐药葡萄球菌、链球菌、肠球菌。
肝硬化患者因免疫力低下、下肢水肿等原因易并发下肢蜂窝织炎,以革兰阴性杆菌为主。ESLD患者长期卧床易并发皮肤软组织化脓性感染,以金黄色葡萄球菌为主。除了依据病原体类型、耐药率、组织渗透性尽早经验性抗感染治疗,外科干预也至关重要。
侵袭性真菌感染(invasive fungal infection,IFI)在ESLD患者中常见于呼吸道、泌尿道、腹腔、血流,也可见于颅内及皮肤软组织等,以念珠菌属和曲霉属为主,念珠菌属主要是白色念珠菌,常见于血流、腹腔、泌尿道,曲霉菌属则主要是烟曲霉,常见于肺部,此外,隐球菌可见于颅内真菌感染。抗真菌药物选择如表1所示。
表1 ESLD患者抗真菌药物选择
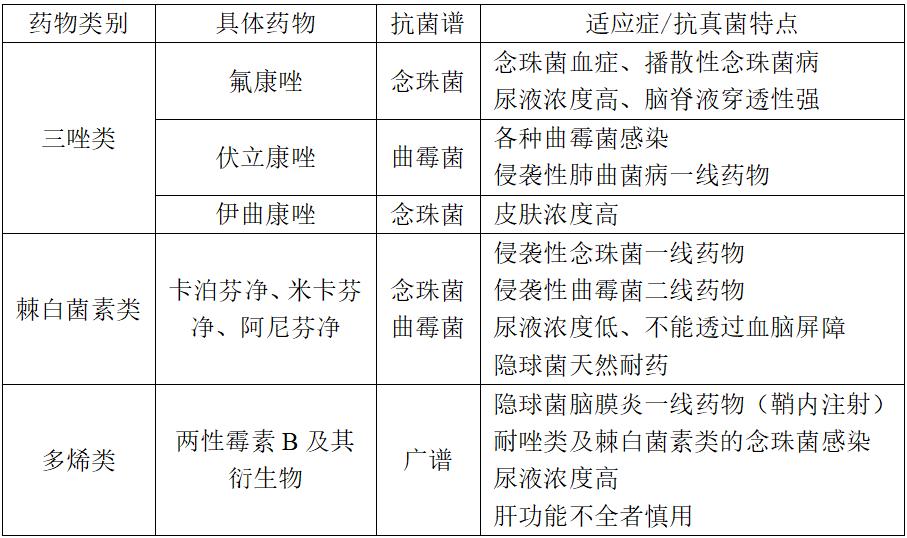
ESLD感染早期临床表现多不典型,但实验室指标CRP、PCT、中性粒细胞淋巴细胞比值可用于识别ESLD细菌感染高风险患者,由于细胞因子白细胞介素(interleukin,IL)-6可增加肠道通透性易致菌群移位、IL-11可抑制免疫细胞清除细菌,血清球蛋白(globulin,GLB)与免疫系统活性呈正相关,因而也具有一定预测细菌感染发生的价值。基于GLB、IL-6和CRP构建的GIC模型,对HBV相关ACLF患者7天细菌感染发生风险预测效果良好(灵敏度、特异度均达75%),可应用于临床协助开展早期预防和经验性抗感染治疗。
《中国医学论坛报》版权所有,转载须授权
【猜你想看】
查看更多