




密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过






胡瑾华 主任医师
肝病医学部 | 解放军总医院第五医学中心
错过等一年,点击图片参与活动↓↓↓
重症肝病合并侵袭性真菌感染(IFI)预后差,临床表现常不典型,而抗真菌药物又多在肝脏代谢,毒副作用大,临床诊治困难。中国研究型医院学会肝病专业委员会重症肝病学组和中华医学会肝病学分会重症肝病与人工肝学组组织国内肝病、感染、微生物学、临床检验等相关专家,以解决临床实际问题为出发点,紧紧围绕重症肝病合并IFI临床特点、诊断、治疗进行多次讨论,提出17条推荐意见,形成《重症肝病合并侵袭性真菌感染诊治专家共识》(以下简称《共识》),以供医务人员在临床实践中提供参照和指导。《中国医学论坛报》特邀牵头专家胡瑾华教授撰写《共识》解读,以期更好地指导重症肝病合并侵袭性真菌感染的规范化治疗。
作者:解放军总医院第五医学中心 胡瑾华 袁婧

胡瑾华教授
研究显示,重症肝病合并IFI的发生率可达15%。IFI在重症肝病患者中最常见的感染部位是肺,占37%~56%,其他部位报道较多的分别为消化道、泌尿道、腹腔、血流等。重症肝病合并IFI最常见的致病真菌有念珠菌属和曲霉属。白念珠菌是肠道、血流、腹腔、泌尿道的主要致病菌,占念珠菌属50%以上。曲霉属是肺部IFI的主要致病菌,其中烟曲霉最常见。隐球菌是中枢神经系统真菌感染的重要致病菌(A1)。
本共识将重症肝病患者界定为IFI发生的高危人群。如合并以下情况之一则定义为极高危人群:① 合并营养不良、慢性阻塞性肺疾病、糖尿病、免疫缺陷及肾功能不全接受肾脏替代治疗;② 使用糖皮质激素、免疫抑制剂、广谱抗菌药物治疗;③ 入住重症监护病房;④ 接受侵入性诊疗操作(A2)。
明确重症肝病患者为IFI高危人群,有利于简化临床诊断,提高可操作性。极高危人群抗真菌治疗时机是否应该靠前,是否应该进行抗真菌预防治疗尚存争议,虽然目前尚无循证依据,但对此类人群进行界定可以为未来的临床研究提供参考和方向。
重症肝病合并IFI临床表现常不典型,常见的IFI感染具备其独有的特点:
重症肝病合并IFI的临床表现缺乏特异性,多见于肺部感染,其中又以侵袭性肺曲霉病(IPA)最常见。IPA患者常存在发热、咳嗽、咳黏痰或痰中带血等症状。临床诊断IPA的重要参考依据是胸部CT的影像学特征性表现,如伴或不伴晕征的结节病灶(>1 cm)或楔形坏死病灶、空气新月征和空洞等。推荐对于基础肝病治疗恢复不佳或出现反复,伴发热或其他感染症状、体征,抗细菌药物治疗无效的患者,要积极行胸部CT检查及IFI相关实验室检查,排查真菌感染(B1)。
念珠菌血症是侵袭性念珠菌感染最常见的表现形式,除了典型菌血症临床表现,全身症状呈进行性加重,多表现为肝功能持续恶化、黄疸加深,感染性休克比例高,严重影响预后。放置静脉导管的重症肝病患者出现发热或疾病进展应常规监测筛查真菌感染(B1)。
腹腔真菌感染常合并细菌感染,临床症状与细菌性腹膜炎相似,但腹膜刺激征不典型,可有淡红色血性腹腔积液。临床上对于症状体征不典型、血性腹水、且抗细菌治疗效果不佳的难治性腹膜炎患者,需排查真菌性腹膜炎,必要时给予经验性抗真菌治疗(B2)。
与国际国内各大真菌指南一致,本共识采用确诊、临床诊断、拟诊三个层次诊断,但通过表格1、2列出常用于确诊或临床诊断的微生物及组织学诊断依据,使得临床医师在工作中更易掌握和操作。
表1 用于确诊重症肝病合并IFI的真菌微生物学证据

表2 用于临床诊断重症肝病合并IFI的真菌微生物学证据

(注:内容节选自《重症肝病合并侵袭性真菌感染诊治专家共识》)
确诊指重症肝病患者具备可能感染部位的临床特征或具备典型影像学特征性改变;同时存在可用于确诊IFI的真菌微生物学检查证据(参考表2)。总体原则即在正常无菌部位或感染灶,通过无菌技术获取的样本经真菌微生物学检查结果阳性,具有真菌感染确诊价值。支气管镜肺泡灌洗液真菌微生物学检查、半乳甘露聚糖(GM)试验有助于肺IFI诊断(B1)。血液、脑脊液隐球菌荚膜多糖体抗原检测阳性可用于隐球菌感染的确诊(A1)。
临床诊断指重症肝病患者具备可能感染部位的临床特征或具备典型影像学特征性改变;同时具备至少一项可用于临床诊断IFI的真菌微生物学检查证据(参考共识表3)。
表3 常见重症肝病合并IFI的治疗药物选择
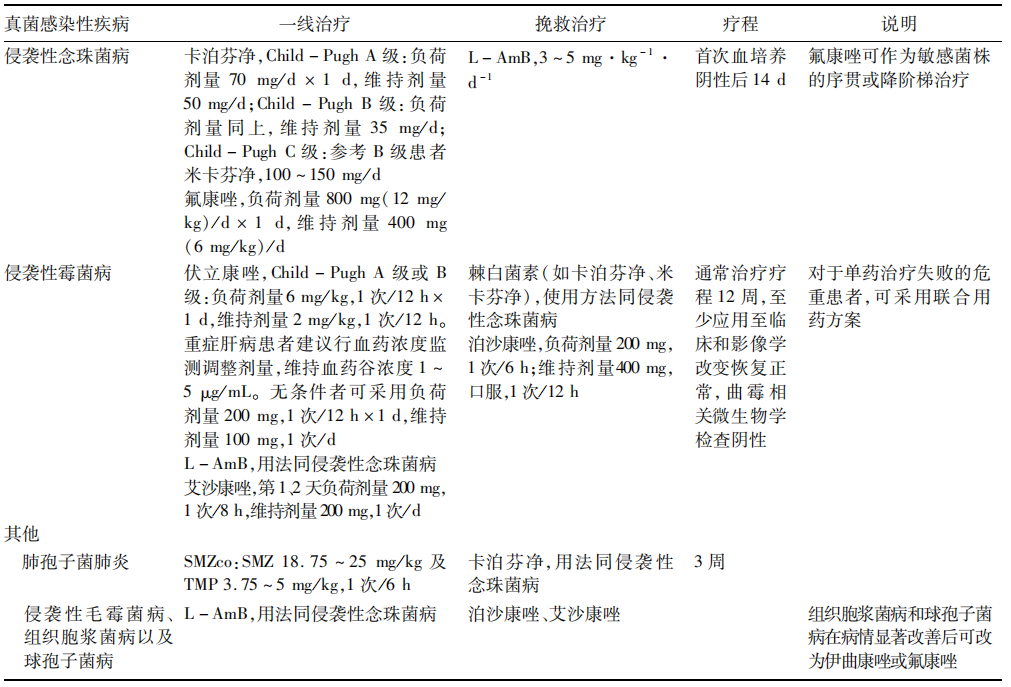
(注:内容节选自《重症肝病合并侵袭性真菌感染诊治专家共识》)
拟诊指重症肝病患者具备可能感染部位的临床特征或具备典型影像学特征性改变。
重症肝病合并IFI的治疗分为经验性治疗、抢先治疗及目标治疗,分别对应拟诊、临床诊断及确诊患者。重症肝病合并IFI患者,应根据临床诊断进行抢先治疗(B1)。若重症肝病患者具有感染的临床表现和特征、经规范的抗细菌治疗无效,病情进一步恶化,可考虑开始抗真菌经验性治疗(C2)。
重症肝病合并侵袭性念珠菌感染推荐棘白菌素为一线治疗药物。氟康唑可作为敏感菌株的降阶梯治疗选择。治疗疗程为抗真菌治疗首次血培养阴性后14 d(B1)。
伏立康唑、两性霉素B脂质体(L-AmB)为重症肝病合并侵袭性肺曲霉病(IPA)的一线用药。使用伏立康唑时,应进行血药浓度监测指导剂量调整(A1)。如无条件,可采用伏立康唑负荷剂量减半至200 mg,每12小时1次,维持剂量100 mg,1次/d的治疗方案(B2)。通常治疗疗程12周,至少应用至临床和影像学改变恢复正常,曲霉微生物学检查阴性(B2)。可采用联合用药方案或棘白菌素作为联合挽救治疗备选药物(A1)。
侵袭性曲霉感染依据最新临床医学证据提出治疗意见,是本《共识》的最大亮点,是对重症肝病治疗禁区的最大突破,已达到国际先进水平。
复方磺胺甲噁唑(SMZco)是肺孢子菌肺炎的首选治疗药物,联合卡泊芬净可能获得更好疗效(B1)。L-AmB是侵袭性毛霉菌病、组织胞浆菌病、球孢子菌病及隐球菌性脑膜炎的首选治疗药物(B1)。
临床应用高效价免疫球蛋白可能提高抗真菌疗效。胸腺肽α1临床用于预防及抗真菌治疗仍需更多临床循证医学数据。此外,过继性T淋巴细胞疗法(ACT)、嵌合抗原受体(CAR)T细胞疗法、粒细胞输注等仍处于临床测试治疗阶段。
重症肝病合并IFI患者近期病死率显著增加,其中侵袭性曲霉感染预后最差,影响预后因素包括年龄、患者肝功能状态、抗真菌治疗疗效等(B2)。
不推荐重症肝病患者给予常规预防性抗真菌药物治疗(A1)。对于极高危人群加强口腔卫生护理,2%~5%碳酸氢钠漱口4次/d,能有效减少口咽部念珠菌感染,进而减少IFI发生的风险(C2)。
肝移植术后患者合并IFI风险较高,念珠菌性血流感染最常见(A1)。肝移植术后患者有高危因素时给予抗真菌药物预防治疗可降低IFI发生的风险(A1)。氟康唑是预防肝移植患者侵袭性念珠菌感染的首选用药(A2),唑类或棘白菌素类药物较L-AmB更具临床优势(A1)。
存在曲霉感染风险的肝移植术后患者应进行靶向抗真菌药物预防治疗,推荐标准剂量的卡泊芬净、米卡芬净、阿尼芬净,或伏立康唑,疗程14~21d(A1) 。
肝移植术后抗真菌预防用药应充分考虑抗真菌药物与抗排异免疫抑制剂之间的相互作用,同时进行抗真菌药物与免疫抑制剂的药物浓度监测,合理调节用药剂量(A1) 。
重症肝病合并IFI未来需要解决以下5个重要问题:① 需要开展多中心前瞻性临床研究:重症肝病患者抗真菌药物治疗时机、安全有效的抗真菌治疗方案及疗程;② 开发早期诊断技术和方法;③ 寻找重症肝病合并IFI精准预后预测及治疗监测的指标;④ 开展极高危人群预防及治疗时机的临床研究;⑤ 研发新型不良反应小、治疗效果佳的抗真菌和免疫治疗药物,进一步提高重症肝病合并IFI的防治水平。
(本文版权属于中国医学论坛报社,转载需授权)
猜你想看





